2025年10月20日,再鼎医药在ClinicalTrials.gov网站上注册了其创新型DLL3靶向抗体药物偶联物(ADC)ZL-1310治疗晚期小细胞肺癌(SCLC)的全球III期临床试验。该研究计划入组665例患者,预计于2028年11月初步完成。
ZL-1310采用新一代ADC技术平台TMALIN®构建,利用人源化抗DLL3单克隆抗体与拓扑异构酶I抑制剂(camptothecin衍生物)通过可裂解连接子连接,旨在提高药物在肿瘤微环境中的递送效率,克服传统ADC疗法的局限性。
在2025年美国临床肿瘤学会(ASCO)年会上,ZL-1310的最新临床数据引起广泛关注。在一项全球多中心III期临床试验中:
ZL-1310在二线SCLC患者中的客观缓解率(ORR)为67%;在1.6 mg/kg剂量组中,ORR为79%;
在二线及以上SCLC患者中,ORR为68%;在脑转移患者中,ORR为68%。
在安全性方面,ZL-1310在小细胞肺癌二线治疗中保持极具竞争力的安全性和疗效特征。
鉴于ZL-1310在晚期小细胞肺癌患者中的优异疗效和良好安全性,再鼎医药计划于2026年在美国提交加速批准上市申请。此外,公司还在探索ZL-1310在一线小细胞肺癌和其他神经内分泌肿瘤适应症中的应用。
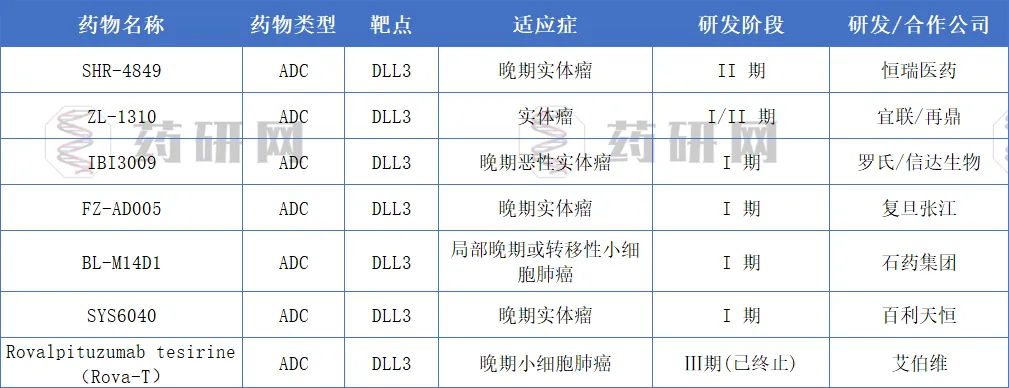
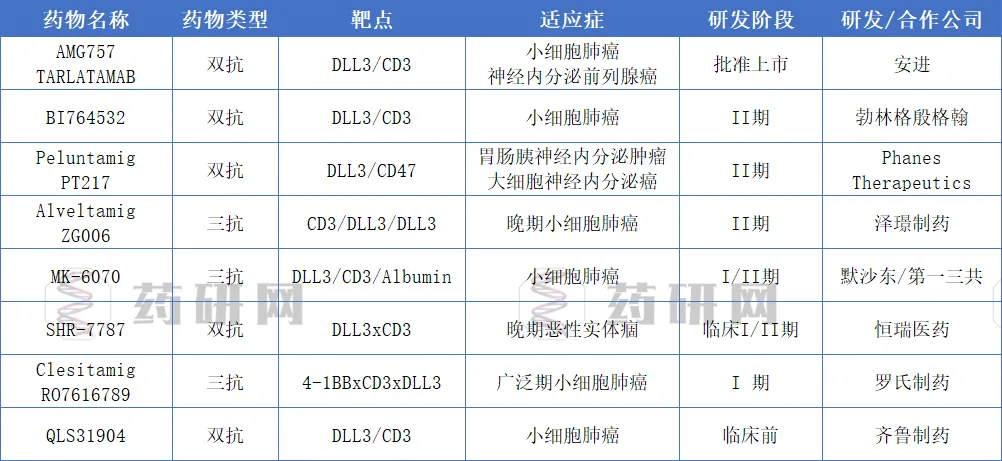
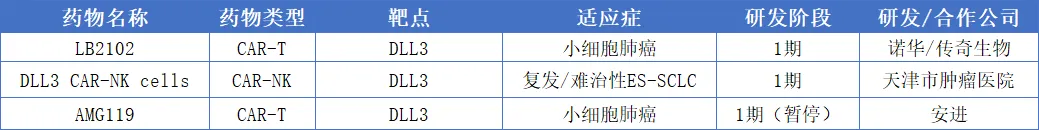
全球DLL3研发呈现快速发展态势,策略涵盖双特异性T细胞接合剂(BiTE)、抗体-药物偶联物(ADC)以及CAR-T/CAR-NK免疫疗法,为小细胞肺癌等神经内分泌肿瘤的精准治疗带来了新的希望。
中国药企在DLL3赛道表现突出,贡献全球 60% 以上管线,覆盖双抗、三抗、ADC、CAR-T、CAR-NK等多类型药物,尤其在ADC和细胞疗法上具领先潜力,蕴藏丰富BD大单机会。随着更多疗法上市和临床推进,DLL3 有望为小细胞肺癌患者带来生存获益,同时为全球药企提供战略和资本布局机遇。点击了解DLL3相关产品