靶点专栏
由国际肺癌研究协会主办的2025年世界肺癌大会(WCLC)于9月6日至9日在西班牙巴塞罗那召开。在本次会议上,由百利天恒自主研发的全球首创EGFR×HER3双特异性抗体药物偶联物(ADC)iza-bren(BL-B01D1)治疗非小细胞肺癌(NSCLC)的两项研究数据公布并进行了口头报告,进一步验证了 iza-bren 在 EGFR 突变肺癌人群的积极疗效,展现了巨大的临床应用潜力与可靠性。
靶点简介
ERBB受体家族包含四个成员(EGFR/HER1、HER2、HER3和HER4),它们在多种癌症中异常激活,已成为精准治疗的重要靶点。
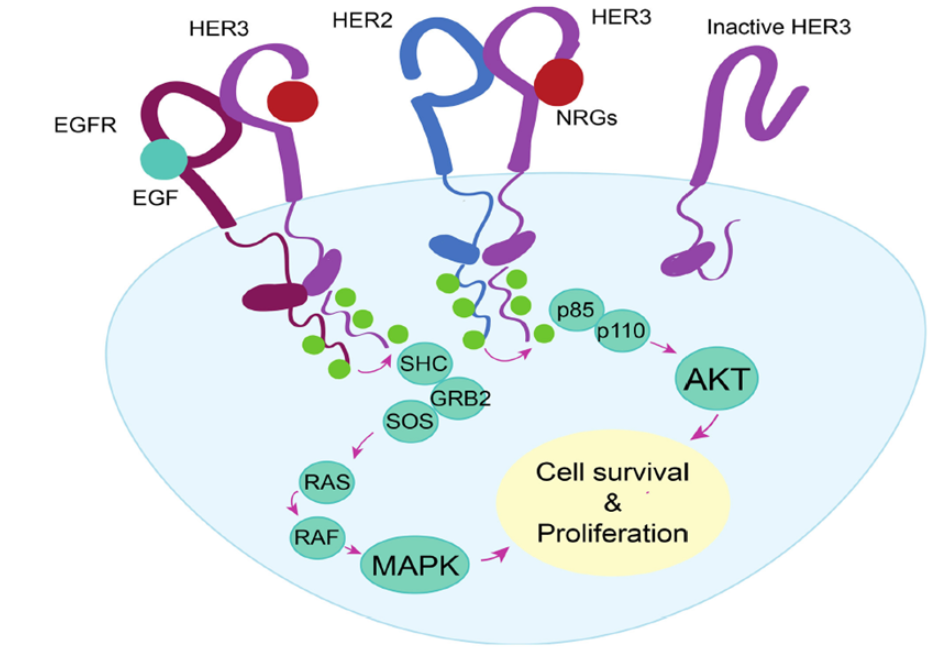
HER3二聚体及其介导的信号转导级联
EGFR具有完整的酪氨酸激酶活性,通过与配体结合引发二聚化,激活RAS-RAF-MEK-ERK和PI3K-AKT-mTOR等下游信号通路,促进肿瘤细胞增殖和转移 [3]。
HER3因其激酶结构域缺陷曾被认为治疗价值有限,但研究发现它是EGFR家族中不可或缺的二聚化伴侣[4]。HER3拥有六个PI3K结合位点,是激活PI3K-AKT通路最有效的ERBB成员。在EGFR-TKI治疗过程中,肿瘤细胞通过以下机制介导耐药:与MET、AXL等受体形成异源二聚体;上调HER3表达;激活heregulin等配体自分泌环[5]。
特别重要的是,EGFR与HER3可形成功能互补的异源二聚体:EGFR提供激酶活性,HER3提供信号接头蛋白结合位点,协同激活PI3K/AKT和MAPK通路,促进肿瘤进展[6]。这一机制为同时靶向两个受体提供了理论基础,通过协同抑制可有效克服单一靶向治疗的耐药问题[7]。
靶向治疗的发展与瓶颈
EGFR靶向治疗主要包括靶向胞内激酶结构域的小分子抑制剂(TKIs)和靶向胞外区的单克隆抗体。TKIs通过竞争性抑制ATP结合,阻断EGFR自身磷酸化和下游信号传导[8]。
目前EGFR-TKI已发展至第四代,其中第三代药物奥希替尼成为一线标准治疗,中位无进展生存期(mPFS)达18.9个月[12]。然而,获得性耐药仍是主要挑战,C797S突变约占耐药机制的15-20%[9]。
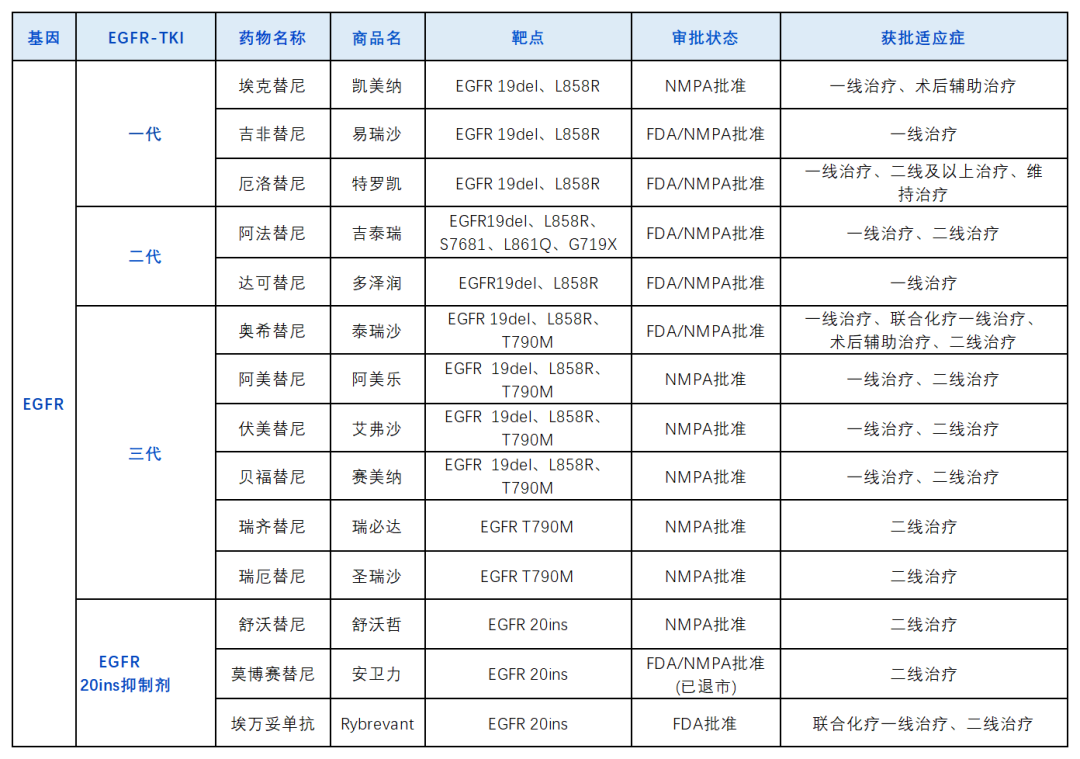
已获批上市的EGFR-TKI靶向药物
超越传统联合:双特异性抗体引领治疗新范式
近年来出现的创新联合策略,如免疫+化疗+抗血管生成四药联合、双特异性抗体+化疗三药联合以及ADC药物,将mPFS提升至6.3-7.2个月,但仍未满足临床需求[11]。双特异性抗体通过同时靶向EGFR和HER3,为克服耐药提供了新思路。
此次WCLC公布了一项iza-bren单药治疗经治EGFR突变晚期NSCLC患者的I/II期研究。在171例入组患者中,大会重点报告了50例仅既往接受过EGFR-TKI(未化疗)患者的数据,该人群接受2.5 mg/kg剂量治疗。结果显示,中位无进展生存期(mPFS)达12.5个月,中位缓解持续时间(mDoR)为13.7个月。中位随访20.5个月,中位总生存(mOS)尚未达到,12个月OS率为80.3%。
来自中山大学肿瘤防治中心的方文峰教授汇报指出:第三代EGFR-TKI目前是EGFR突变NSCLC的标准一线治疗,但几乎所有患者都会出现耐药,后续治疗选择有限,mPFS通常仅4-6个月。该研究mPFS达12.5个月,是迄今为止报道的ADC药物中最长的mPFS[1]。
目前在研的靶向EGFR x HER3双抗ADC已经有14款,处于临床阶段的有6款,涉及百利天恒、映恩生物、君实生物、信达生物等ADC领域知名企业。
小 结
EGFR与HER3在非小细胞肺癌的发生发展和耐药机制中具有重要作用。
EGFR驱动肿瘤增殖,而HER3作为关键的二聚化伙伴,强力激活PI3K/AKT等下游信号通路。两者形成的功能互补性异源二聚体,成为克服EGFR-TKI耐药的重要靶点。
EGFR×HER3双特异性药物如iza-bren等的开发,不仅证实了协同阻断的科学价值,也为延长患者生存带来了新的希望。随着临床研究的深入,双靶向治疗有望为EGFR突变NSCLC患者提供更有效和持久的治疗选择。
用心做好细胞,为更好的靶向药
吉满生物精准把握市场需求与科研前沿,推出EGFR/HER3靶点相关细胞系、抗体、蛋白及HER3-DXd阳性参照产品。产品覆盖药物研发全过程,全面支持抗体筛选、表征及一致性评价,助力药企加速抗体药物的研发进程,推动临床申报。(详情咨询吉满客服:18916119826)此处点击了解EGFR/HER3相关产品
靶点相关细胞系:适用于药物功能筛选、活性评价、药效学研究及信号通路验证
高活性重组蛋白:满足结合分析、筛选及免疫研究需求
高特异性抗体: 提供经严格验证的抗体产品,支持流式细胞术、免疫组化、Western Blot、ELISA 等多种检测应用,确保实验结果准确可靠
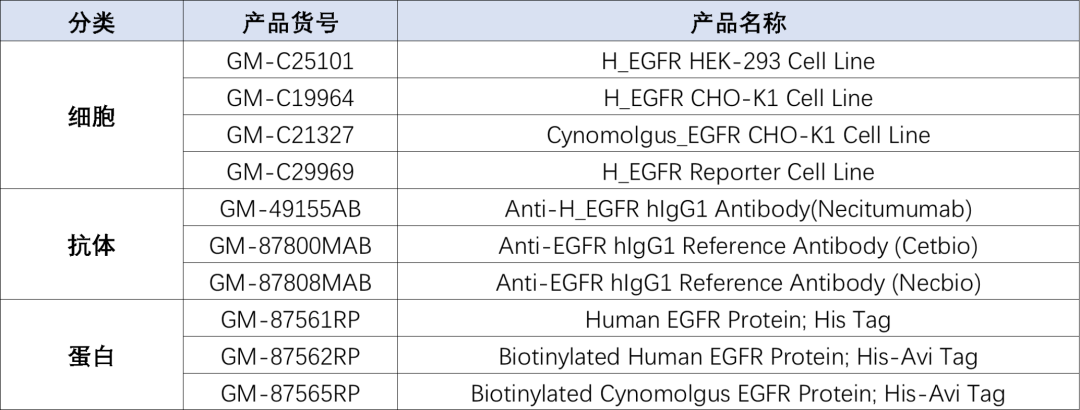
EGFR产品列表(部分)
HER3产品列表
数据展示(部分)
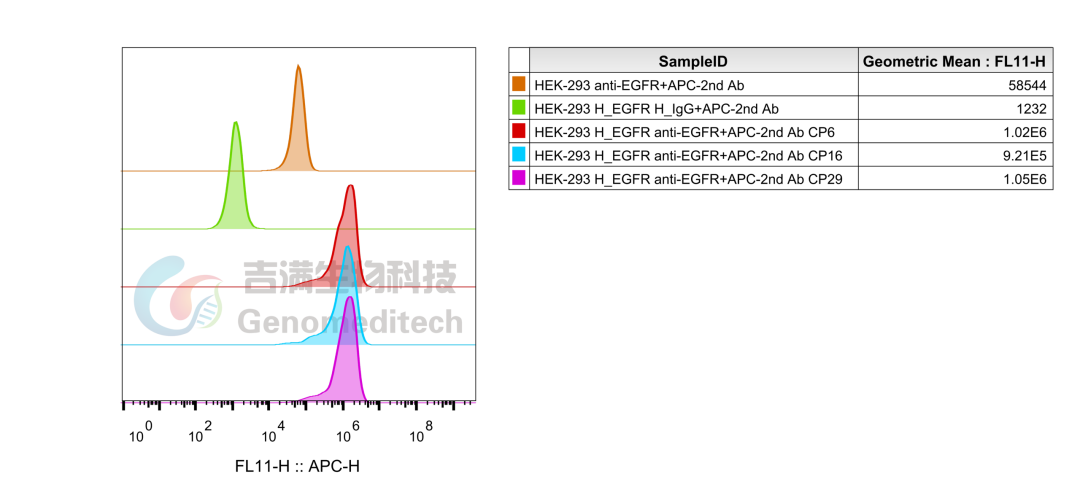
GM-C25101:H_EGFR HEK-293 Cell Line
该产品经过29代验证仍稳定表达,助力抗体筛选、表征及一致性评价,高效推进抗体药物研发与临床申报
使用Anti-H_EGFR hIgG1 Antibody稳定性验证结果
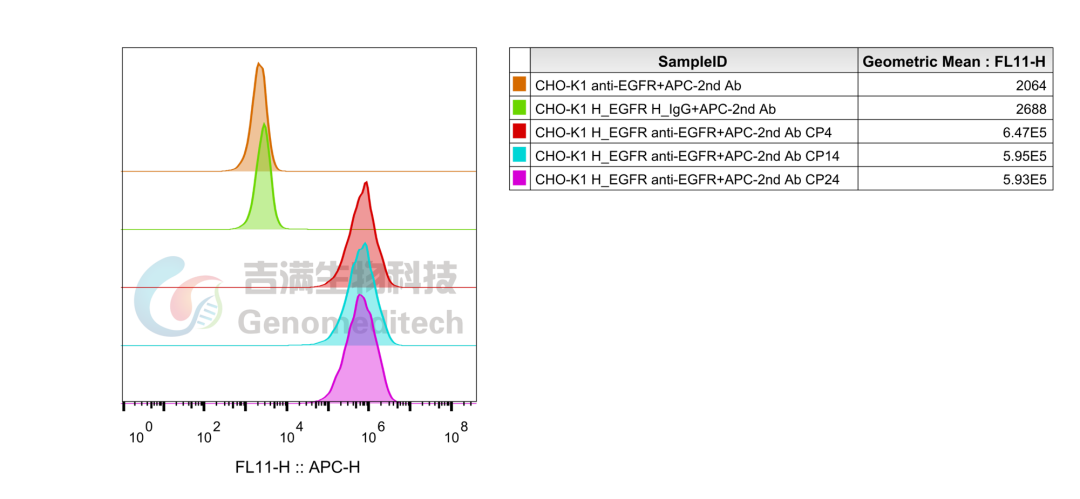
GM-C19964:H_EGFR CHO-K1 Cell Line
使用Anti-H_EGFR hIgG1 Antibody稳定性验证结果
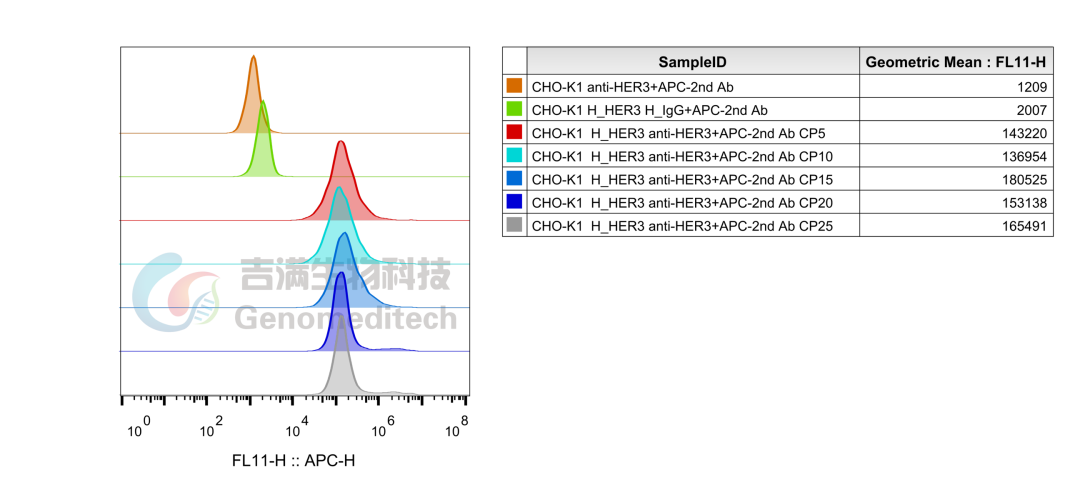
GM-C12969:H_ERBB3(HER3) CHO-K1 Cell Line
该产品经过25代验证仍稳定表达,助力抗体筛选、表征及一致性评价,高效推进抗体药物研发与临床申报
使用Anti-H_ERBB3(HER3) hIgG1 Antibody稳定性验证结果
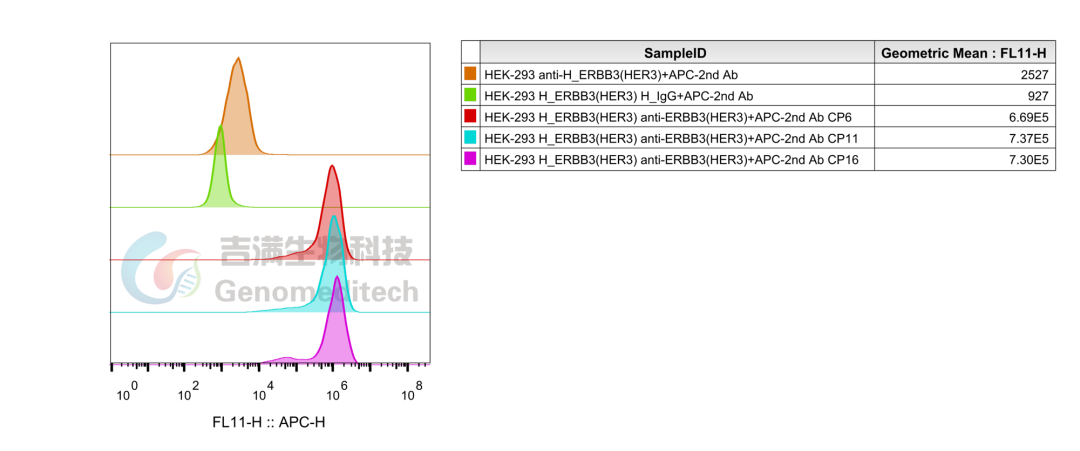
GM-C34144:H_ERBB3(HER3) HEK-293 Cell Line
使用Anti-H_ERBB3(HER3) hIgG1 Antibody(Barecetamab)稳定性验证结果
联系我们
吉满生物专注为生物药开发,提供高效的研发工具和解决方案。截止当前已布局近400个热门靶向药靶点,超1000株现货单克隆细胞系,涵盖肿瘤相关抗原(TAA)、 免疫检查点、Fc受体、细胞因子和激酶等热门靶点类型。旨在助力、加速大分子早期研发,做到进口细胞的国产替代。同时构建了丰富的蛋白、抗体及试剂现货产品库。
参考资料:
[1]Fang W, et al. Updated efficacy and safety of BL-B01D1, a first-in-class EGFRxHER3 bispecific antibody-drug conjugate (ADC), in patients with previously treated EGFR-mutant non-small cell lung cancer (NSCLC). Presented at: 2025 World Conference on Lung Cancer; September 6-9, 2025; Barcelona, Spain. Oral Presentation.
[2]Zhou F, et al. BL-B01D1 in combination with osimertinib in patients with untreated EGFR-mutant advanced NSCLC: Preliminary results from a phase II study. Presented at: 2025 World Conference on Lung Cancer; September 6-9, 2025; Barcelona, Spain. Oral Presentation.
[3]Rosell R, Karachaliou N. Large-scale screening for somatic mutations in lung cancer. Lancet. 2016;387(10026):1354-1356.
[4]Campbell MR, Amin D, Moasser MM. HER3 comes of age: new insights into its functions and role in signaling, tumor biology, and cancer therapy. Clin Cancer Res. 2010;16(5):1373-1383.
[5]Engelman JA, Jänne PA. Mechanisms of acquired resistance to epidermal growth factor receptor tyrosine kinase inhibitors in non-small cell lung cancer. Clin Cancer Res. 2008;14(10):2895-2899.
[6]Amin DN, Campbell MR, Moasser MM. The role of HER3 in the resistance of cancer cells to targeted therapies. Expert Opin Investig Drugs. 2010;19 Suppl 1:S67-S78.
[7]Schaefer G, et al. A two-in-one antibody against HER3 and EGFR has superior inhibitory activity compared with monospecific antibodies. Cancer Cell. 2011;20(4):472-486.
[8]Zhang H, et al. EGFR kinase domain mutations and their implications in targeted therapy for non-small cell lung cancer. Front Biosci (Landmark Ed). 2017;22(8):1295-1306.
[9]Leonetti A, et al. Resistance mechanisms to osimertinib in EGFR-mutated non-small cell lung cancer. Br J Cancer. 2019;121(9):725-737.
[10]Hanna N, et al. Systemic therapy for stage IV non-small-cell lung cancer: American Society of Clinical Oncology Clinical Practice Guideline Update. J Clin Oncol. 2017;35(30):3484-3515.
[11]Nakagawa K, et al. Final progression-free survival results from the KEYNOTE-789 study of pembrolizumab plus chemotherapy versus chemotherapy for EGFR-mutant NSCLC. ESMO Congress. 2023; Abstract LBA65.
[13]https://mp.weixin.qq.com/s/WVrduCZsyesxl6-NPUpTYQ