IL-4与IL-13是T辅助细胞2型(Th2)细胞因子家族的核心成员,主要由 Th2 细胞、ILC2、嗜酸粒细胞及肥大细胞产生。
这两种细胞因子通过与其受体复合体结合,激活Janus家族激酶(主要是JAK1与JAK3或JAK1与TYK2),随后磷酸化信号导引和激活剂转录因子6(STAT6),驱动典型的2型免疫反应。[1]
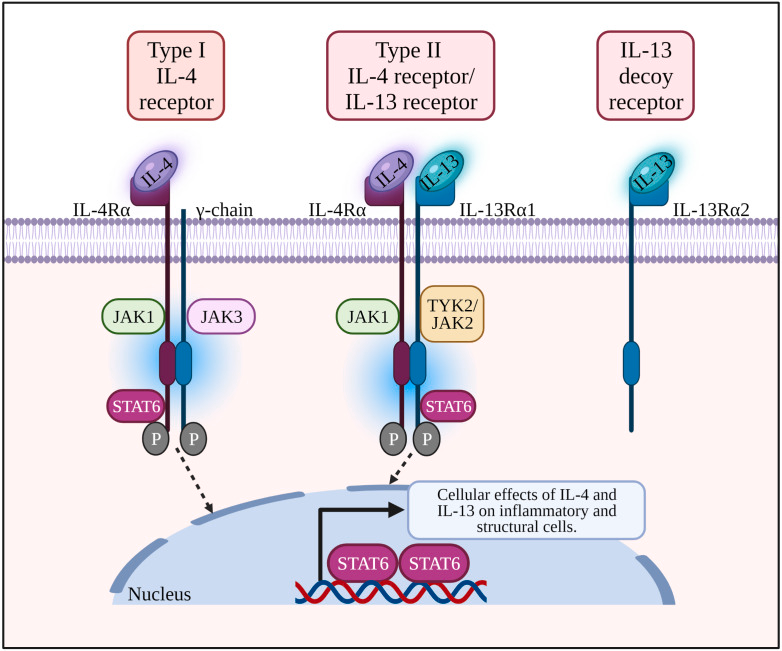
IL-4结合I型受体和II型受体
IL‑4 与 IL‑13受体表达
IL‑4能结合两种受体复合体,而IL-13仅能结合II型受体:
I 型受体(IL‑4Rα/γc):主要表达于造血细胞,介导 IL‑4 诱导 Th0 向 Th2 分化、促进 B 细胞 Ig 类别转换为 IgE,是体液免疫和过敏反应的关键机制。
II 型受体(IL‑4Rα/IL‑13Rα1):IL‑4 与 IL‑13 共用此受体,主要表达于上皮细胞、成纤维细胞和平滑肌细胞等非造血细胞。通过该复合体激活 JAK‑STAT(主要是 STAT6)路径,诱导黏液分泌、黏膜屏障炎症、组织重塑和嗜酸粒细胞募集。
正常情况下,IL-4和IL-13受体亚基在动态平衡条件下低水平表达。作为诱导和维持2型炎症反应的关键细胞因子,它们与多种特应性疾病密切相关,例如特异性皮炎(AD)、哮喘和慢性鼻窦炎伴鼻息肉病(CSwNP)等。
值得注意的是,细胞因子的功能具有环境依赖性。在类风湿关节炎(主要由Th1/Th17驱动)中,IL-4表现出显著的抗炎特性,能抑制滑膜细胞产生IL-1、IL-6、IL-8和TNF-α等促炎因子。
此外,在癌症研究中发现,多种肿瘤细胞(如胶质母细胞瘤、乳腺癌、淋巴瘤等)表面IL-4Rα和IL-13Rα1表达上调,这不仅与肿瘤进展有关,也成为了潜在的免疫治疗靶点。
“追赶者”的集体登场
据Frost & Sullivan报告,全球IL-4Rα靶向疗法的市场规模预计将于2030年达到287亿美元,中国相关市场规模预计将达到40.8亿美元。
目前,国内外企业有众多管线处于临床阶段,主要集中于哮喘和AD两大领域。未来新的适应症和临床应用可能还会不断涌现。下表为部分药物研发现状:
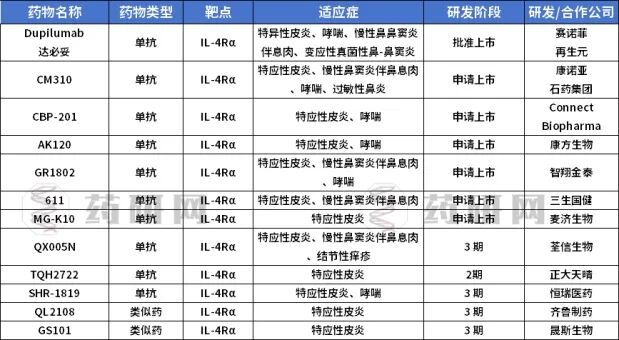
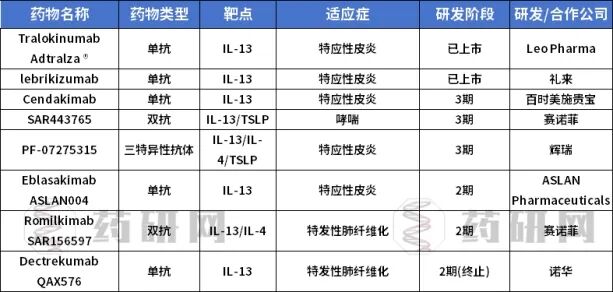
最新药物进展资讯
度普利尤单抗
2月24日,赛诺菲宣布其靶向IL-4Rα的单抗——度普利尤单抗再添新适应症,正式获得美国FDA批准用于变应性真菌性鼻-鼻窦炎(AFRS),成为该领域首个针对性治疗药物。
自赛诺菲与再生元联手推出这款全球首个靶向IL-4Rα的全人源单抗以来,度普利尤单抗的商业曲线几乎一路垂直上升。2024年,度普利尤单抗接力阿达木单抗成为新的“自免药王”后,其2025年销售额已飙升至157.14亿欧元(约合182.91亿美元),再次蝉联该宝座!
小 结
度普利尤单抗的爆发式增长不仅印证了 IL-4/IL-13 作为 2 型炎症核心节点的临床价值,也加速将该通路推向全球免疫治疗研发的主战场。随着更多企业涌入这一赛道,IL-4Rα 正从一家企业的深度布局,演变为整个行业竞逐的战略高地。
与此同时,纳米抗体、口服小分子IL4Rα拮抗剂及IL4Rα靶向ADC等前沿管线虽尚处早期探索期,却已勾勒出该领域未来的长期创新蓝图。
用心做好细胞,为更好的靶向药
吉满生物自主研发了涵盖IL-4/IL-13稳定过表达细胞系、报告基因检测细胞系及高特异高灵敏单克隆抗体的解决方案,全方位赋能药物研发,加速临床申报。
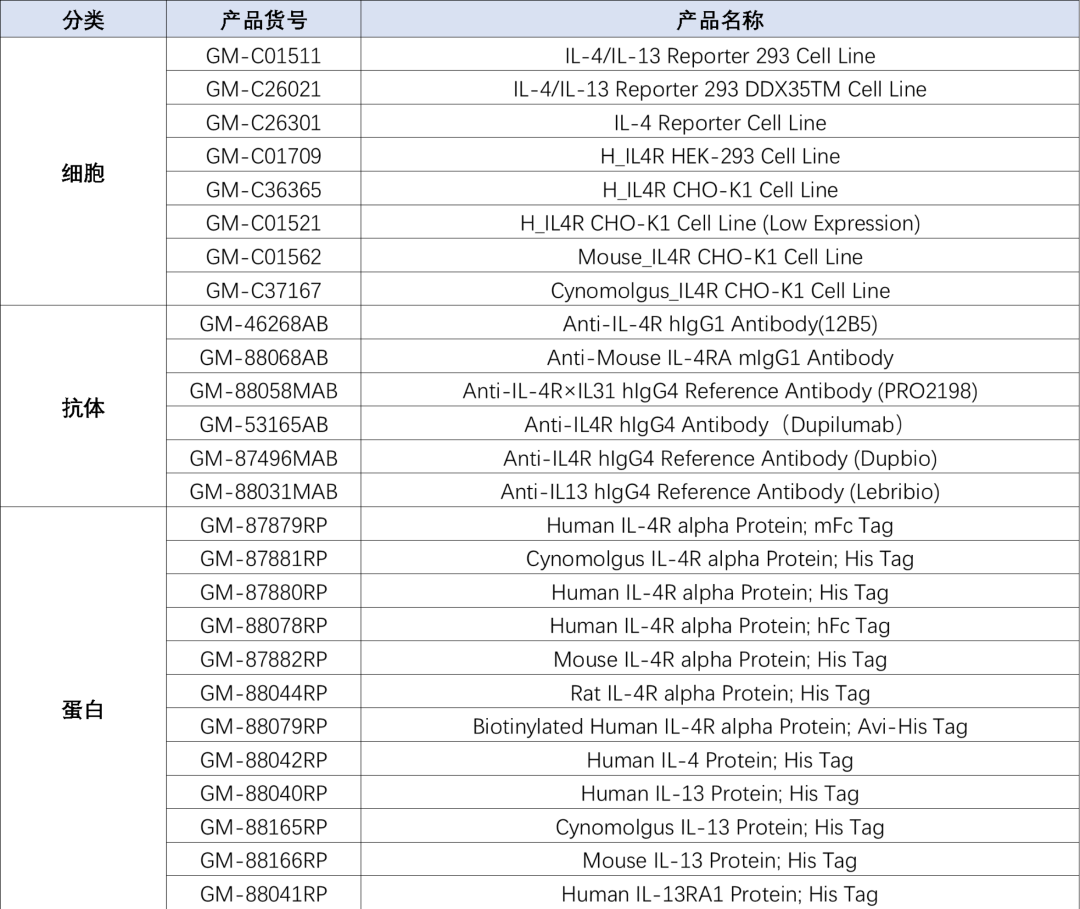
产品列表
细胞产品数据展示(部分)
GM-C01709:H_IL4R HEK-293 Cell Line
经抗体验证,该细胞系产品表达稳定
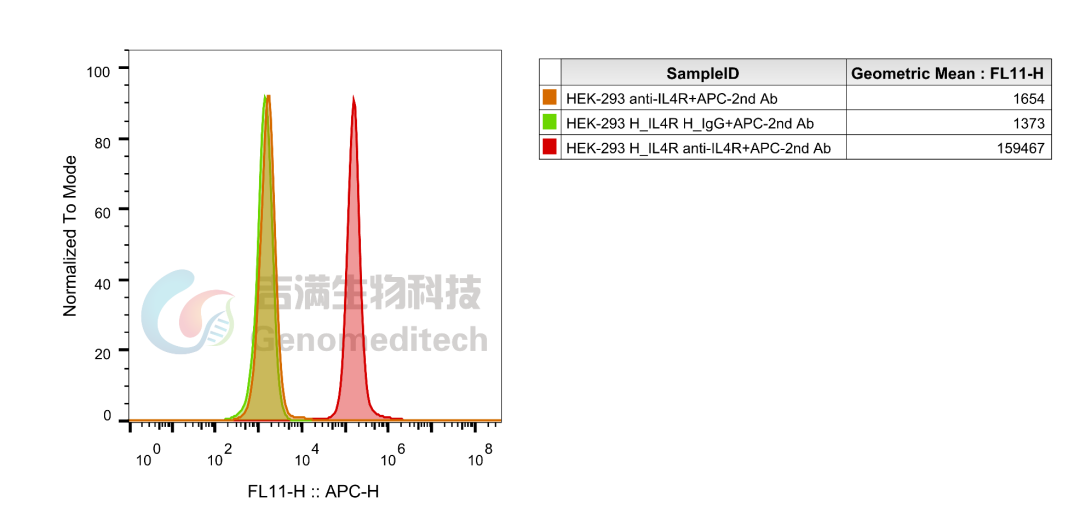
使用Anti-IL4R hIgG4 Reference Antibody (Dupbio)
验证结果
GM-C26021:IL-4/IL-13 Reporter 293 DDX35TM Cell Line
经连续传代 ≥35 代验证,Reporter 信号保持高度稳定,具备卓越的长期实验一致性
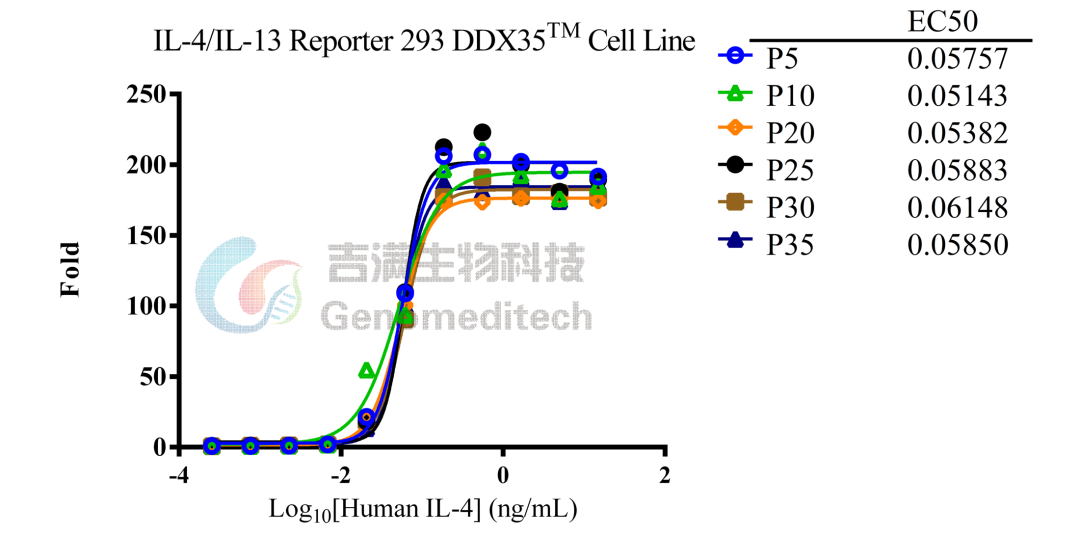
使用Recombinant Human IL‑4验证结果

使用Human IL13 Protein验证结果
蛋白产品Elisa验证(部分)
GM-87880RP:Human IL-4R alpha Protein; His Tag
经ELISA验证蛋白表现出优异的活性,信号强、背景低,可应用于抗体筛选及结合分析等实验。

抗体产品数据验证(部分)
GM-88068AB:Anti-Mouse IL-4RA mIgG1 Antibody
该抗体特异性结合 IL‑4RA,有效阻断 IL‑4/IL‑13 信号,抑制 STAT6 激活。可以用于探索与其他疗法(如免疫检查点抑制剂)的联合应用。
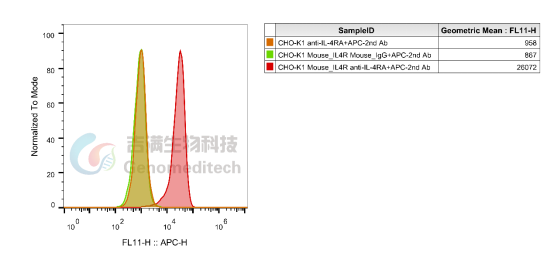
Flow Cytometry 验证结果

ELISA验证