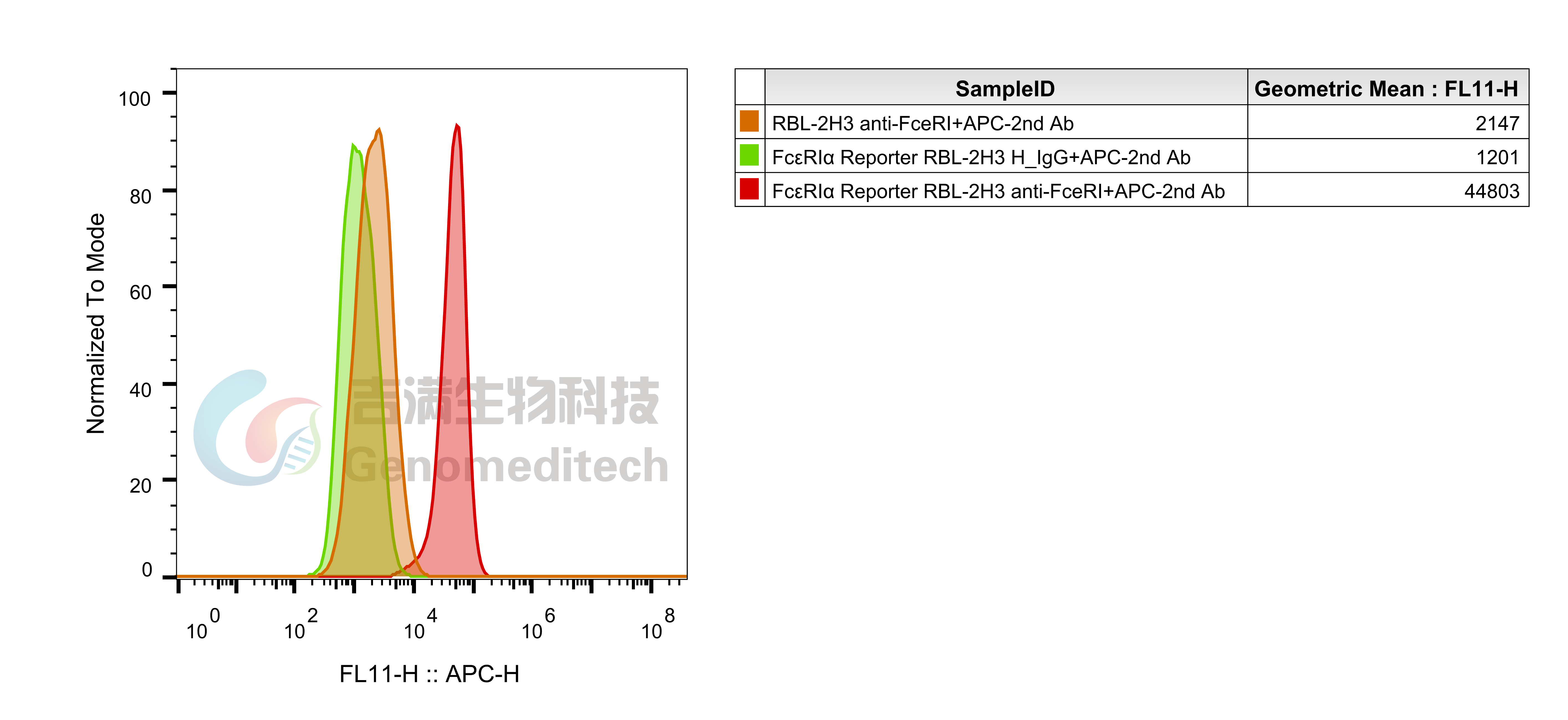
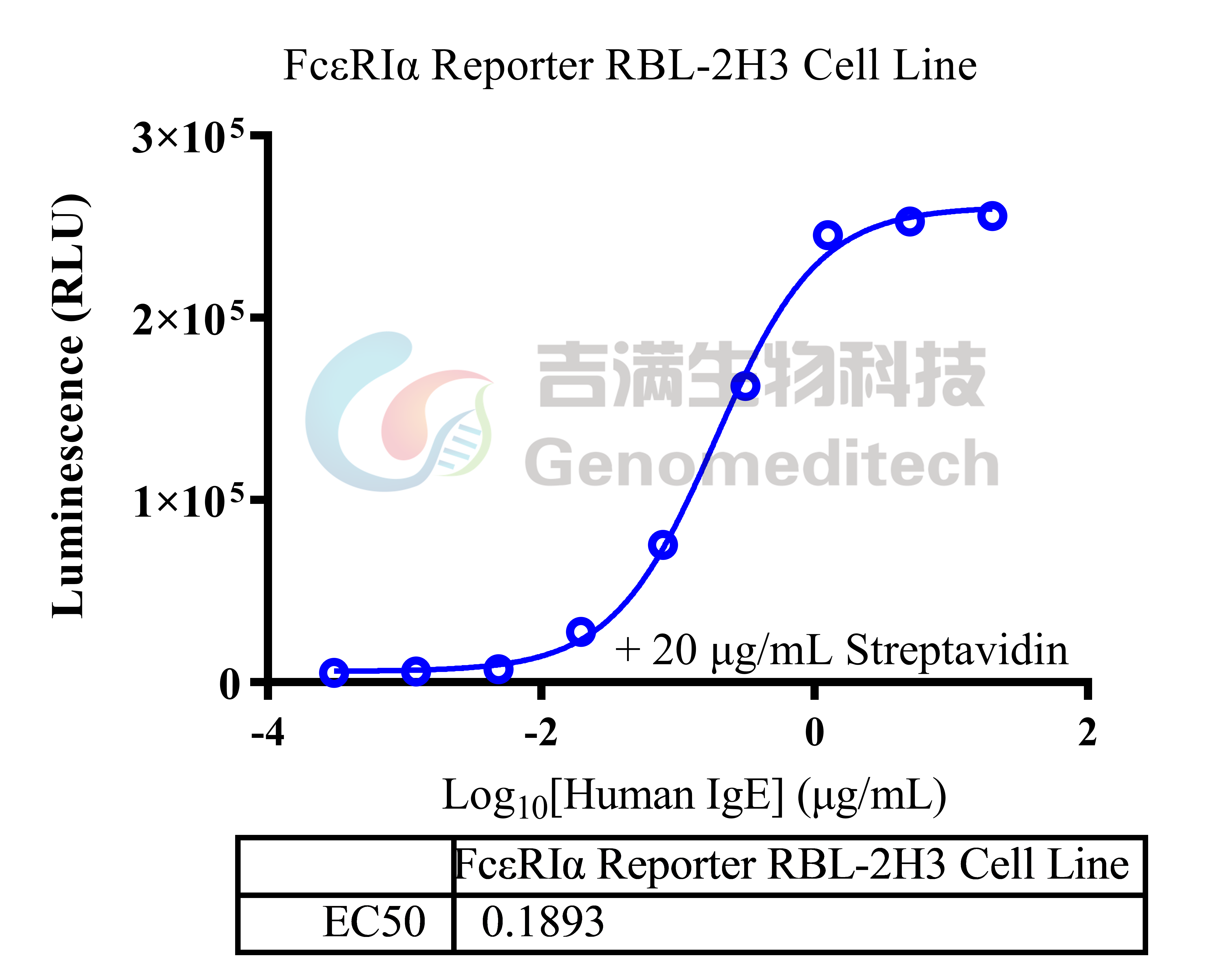
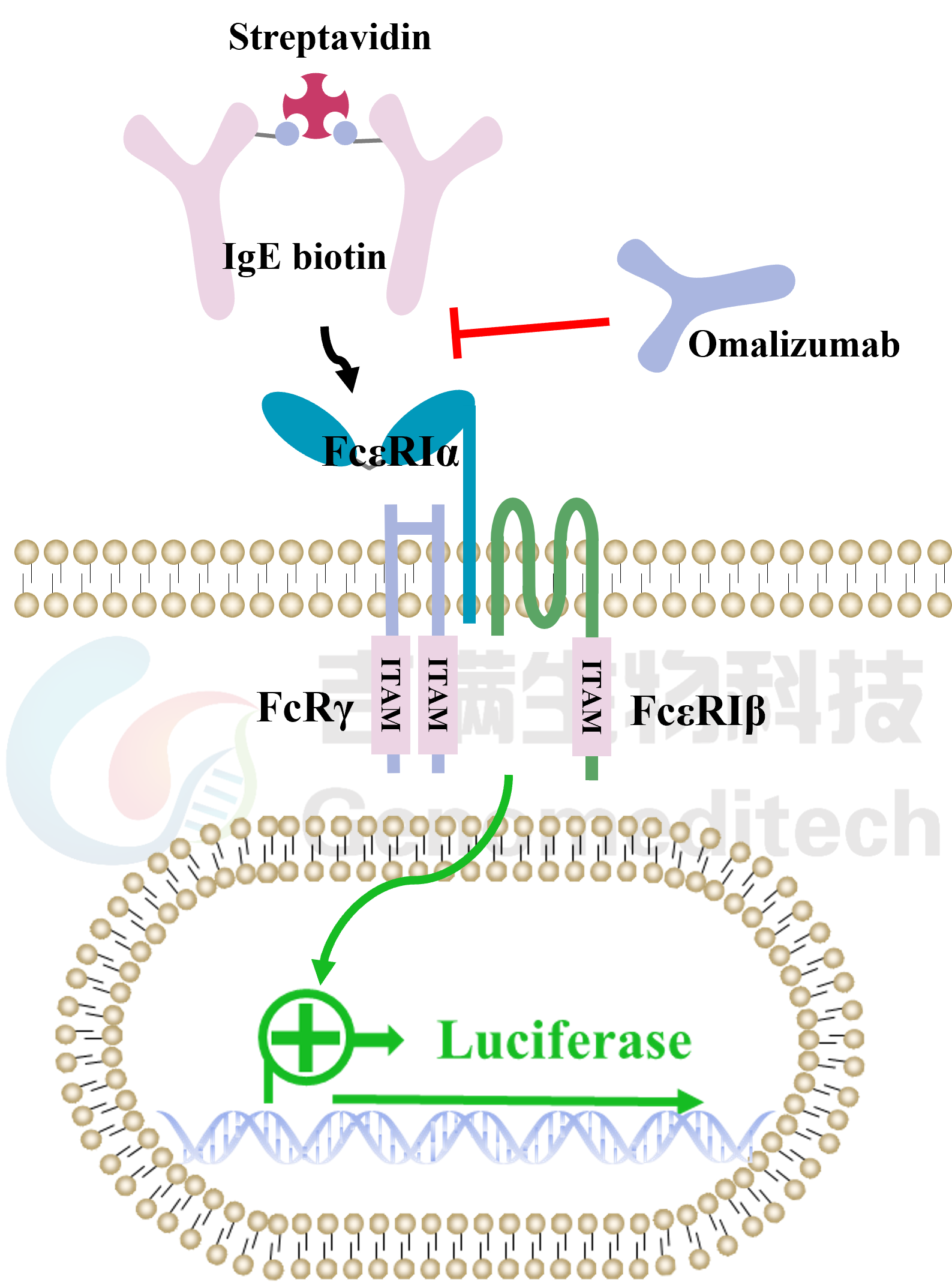
| FcεRIα(高亲和力IgE受体α亚基)是免疫球蛋白E(IgE)的特异性受体,主要表达于肥大细胞和嗜碱性粒细胞表面,在I型超敏反应中起核心作用。该蛋白由胞外区、跨膜区和短胞内尾组成,其胞外区包含两个Ig样结构域(D1和D2),直接结合IgE抗体的Fc段恒定区(Fcε3结构域)。当多价过敏原交联细胞膜上FcεRIα结合的IgE时,会触发受体聚集,激活下游信号通路(如Syk激酶、Ca²⁺内流和NFAT转录因子),导致细胞脱颗粒释放组胺、白三烯等炎症介质。FcεRIα与IgE的结合具有超高亲和力(Kd~10⁻¹⁰ M),这种特性使其成为过敏性疾病治疗的关键靶点,例如抗IgE单抗奥马珠单抗(Omalizumab)正是通过阻断IgE与FcεRIα的结合发挥治疗作用。由于人类细胞系天然缺乏FcεRIα的高表达,研究中常通过转染RBL-2H3大鼠嗜碱性白血病细胞构建模型,用于过敏机制研究和药物筛选。 吉满生物FcεRIα Reporter RBL-2H3 Cell Line是一种Luciferase报告基因细胞系。IgE-biotin通过Fc区与FcεRIα结合,同时其biotin可被链霉亲和素(Streptavidin)交联,模拟过敏原诱导的受体聚集,激活下游信号通路;Omalizumab作为抗IgE单抗,其Fab段特异性结合游离IgE的Fcε3结构域,阻断IgE与FcεRIα的结合,抑制下游信号通路,从而激活荧光素酶(Luciferase)的表达。Luciferase 读值即代表信号通路的激活效果。因此可用于评估抗IgE抗体的生物活性。 |
 |